Tarčno ciljanje metabolizma lipidnih kapljic za učinkovito zmanjševanje odpornosti rakavih celic na stres
Oznaka in naziv projekta
J7-1818 Tarčno ciljanje metabolizma lipidnih kapljic za učinkovito zmanjševanje odpornosti rakavih celic na stres
J7-1818 Targeting lipid droplets to reduce cancer cell resistance to stress
Logotipi ARRS in drugih sofinancerjev

Projektna skupina
Vodja projekta: izr. prof. dr. Toni Petan
Sestava projektne skupine: Povezava na SICRIS
Organizacija prijaviteljica:
Institut Jožef Stefan
Sodelujoče organizacije in raziskovalci:
Kemijski inštitut
prof. dr. Roman Jerala
Medicinska Fakulteta, Univerza v Ljubljani
prof. dr. Mateja Erdani Kreft
Vsebinski opis projekta
Ključni poudarki
- Odpornost rakavih celic na različne oblike stresa je ključna za rast tumorjev in razvoj metastaz.
- Tvorba lipidnih kapljic (LK) in avtofagija se aktivirata pri stresu in omogočata preživetje rakavih celic.
- Avtofagija je lahko vključena tako v biogenezo LK kot tudi v razgradnjo LK (t.i. lipofagijo).
- Naš cilj je opredeliti povezavo med LK in avtofagijo v rakavih celicah izpostavljenih pomanjkanju hranil.
- Z načrtnim ciljanjem te povezave želimo zmanjšati preživetje rakavih celic in vitro in rast tumorjev in vivo.
Povzetek za hitro branje
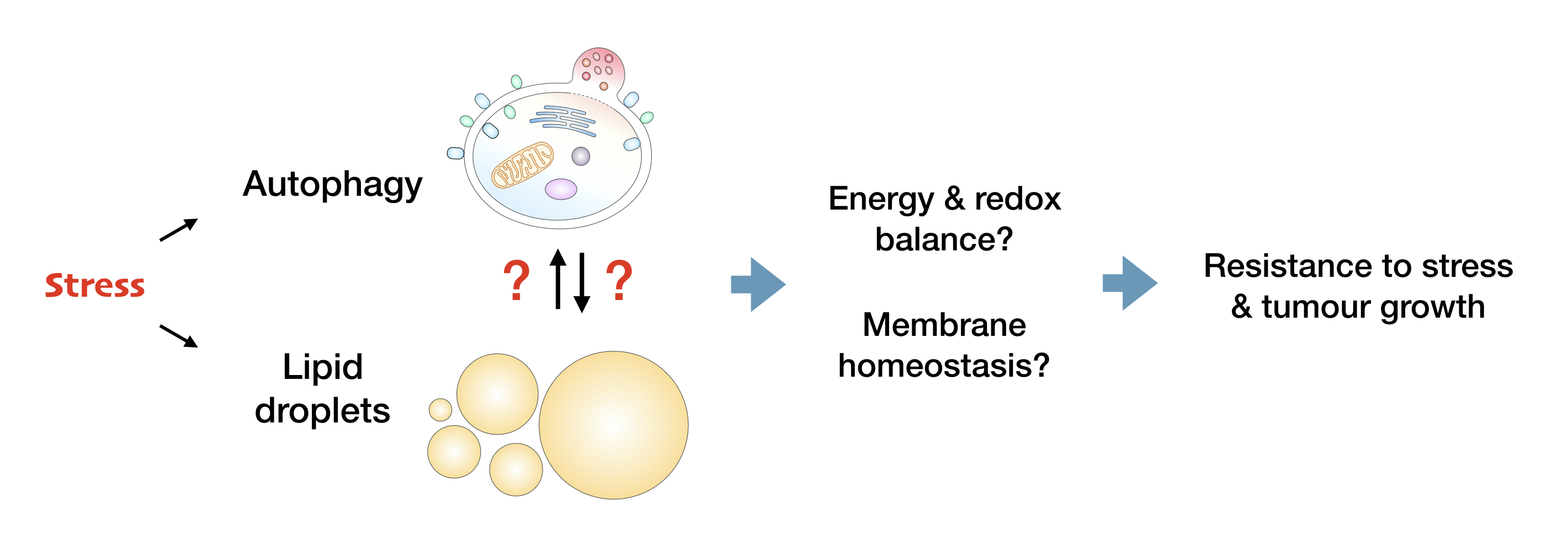
Tvorba lipidnih kapljic in avtofagija se inducirata pri celičnem stresu in prispevata k odpornosti rakavih celic na stres, najverjetneje preko vzdrževanja energetske, redoks in membranske homeostaze. Povezave med avtofagijo in lipidnimi kapljicami pri raku so slabo poznane. Avtofagija je lahko vpletena v sintezo in razgradnjo lipidnih kapljic, lipidne kapljice pa lahko stimulirajo avtofagijo. Naš glavni cilj je razumeti povezave med lipidnimi kaljicami in avtofagijo v rakavih celicah izpostavljenih stresu in ciljati glavne točke teh povezav z namenom onemogočanja preživetja rakavih celic in rasti tumorjev.
Povzetek projekta
- Rakave celice kažejo izjemne sposobnosti adaptacije na stresne pogoje v tumorskem okolju, pri čemer prilagodijo svoj metabolizem glede na razpoložljivost posameznih hranil. Ta metabolična plastičnost je ključna za rast tumorjev, metastaziranje in odpornost na terapijo. Preživetje rakavih celic tekom stresa je odvisno od dostopnosti zunajceličnih lipidov in njihove sposobnosti sintetiziranja, mobilizacije in recikliranja lastnih znotrajceličnih lipidov. Rakave celice lahko dinamično preklapljajo med različnimi viri lipidov, kar je močno otežilo nedavne poskuse, da bi inhibitorje sinteze maščobnih kislin uporabili pri terapiji. Zato je nujno identificirati poti pridobivanja in uporabe lipidov, ki bi jih lahko ciljano inhibirali in s tem znižali odpornost rakavih celic na stres. Lipidne kapljice (LK) so citosolni organeli, ki shranjujejo maščobe in so prisotni v večini celic od kvasovk do človeka. V zadnjem času postaja jasno, da so LK pomembni regulatorji lipidnega metabolizma, transporta in signalizacije. Sinteza LK se inducira v celicah izpostavljenim metaboličnemu in oksidativnemu stresu, kopičijo pa se tudi pri raku. Delujejo kot stikala, ki uravnavajo vnos, shrambo in uporabo lipidov za različne potrebe celice, vključno s proizvodnjo energije, zaščito pred oksidativnim stresom in sintezo membran pri hitri celični delitvi. LK prav tako prevzamejo presežne maščobne kisline in uravnavajo njihovo sproščanje z lipolizo. To blaženje sunkov presežnih lipidov in njihovo naknadno sproščanje je ključna značilnost LK, ki jo rakave celice zlorabijo za zaščito pred stresom. Ciljanje mehanizmov delovanja LK pri rakavih celicah bi torej lahko znižalo njihovo odpornost in omejilo rast tumorjev. Razmerje med metabolizmom LK in avtofagijo, pomembnim mehanizmom celičnega recikliranja in stresnega odgovora, je zapleteno in zaenkrat slabo poznano. Prvič, avtofagija lahko z dovajanjem lipidov pridobljenih z recikliranjem membranskih organelov stimulira sintezo LK. Drugič, avtofagija sodeluje pri razgradnji LK preko njene selektivne oblike imenovane lipofagija. Tretjič, LK lahko vzpodbujajo avtofagijo, tako da dostavljajo lipide nujne za tvorbo avtofagosomov, vzdržujejo homeostazo membran ali stimulirajo signalne poti. Razmerje med LK in avtofagijo lahko torej skriva ključ do dinamike lipidov v rakavih celicah pod stresom. Glavni cilj tega projekta je opredeliti ključne poti, ki povezujejo nastanek in razgradnjo LK z avtofagijo v različnih rakavih celicah z namenom, da bi s tarčnim ciljanjem kritičnih točk na osi LK/avtofagija zmanjšali njihovo odpornost na stres. S preučevanjem vlog glavnih encimov, ki so vpleteni v nastanek in razgradnjo LK v kontekstu aktivirane ali inhibirane avtofagije v različnih pogojih stresa, bomo ugotovili povezave med temi procesi in njihov pomen za preživetje rakavih celic tekom stresa. Z mehanističnimi študijami bomo poskusili določiti načine, preko katerih os LK/avtofagija prispeva k energetski, redoks in membranski homeostazi. To bo tudi prva študija, ki bo zagotovila lipidomski vpogled v medsebojno delovanje avtofagije in lipidno sestavo LK ter sestavo membran tekom stresa. Nenazadnje bomo z uporabo modela mišjega ksenografta prvič ocenili izvedljivost tarčnega ciljanja osi LK/avtofagija za zmanjševanje rasti tumorjev in vivo. Prepričani smo, da bo predlagani projekt odprl nove perspektive pri raziskovanju raka s ciljanjem centralnega lipidnega metabolizma in s stresom povezanega organela – lipidne kapljice.
Osnovni podatki sofinanciranja so dostopni na spletni strani. Povezava na SICRIS.
Faze projekta in opis njihove realizacije
(1) Naš prvi cilj je določiti dinamiko metabolizma LK v rakavih celicah, ki so izpostavljene različnim pogojem stresa in opredeliti vlogo glavnih encimov, ki so vpleteni v biogenezo LK (DGAT1 in DGAT2) in lipolitično razgradnjo (ATGL).
(2) Naš drugi cilj je določiti povezavo med metabolizmom LK in avtofagijo v rakavih celicah izpostavljenih stresu.
(3) Naš tretji cilj je ugotoviti ali je os LK/avtofagija pomembna za preživetje celic tekom stresa in opredeliti glavne celične mehanizme z LK-posredovanega odgovora na stres.
(4) Naš četrti cilj je pokazati, da inhibicija sinteze LK v agresivnih celicah raka dojke zmanjša rast tumorja in vivo.
Bibliografske reference
Jarc, E., Petan, T. (2020). A Twist of FATe: Lipid Droplets and Inflammatory Lipid Mediators. Biochimie 169(), 69-87. https://dx.doi.org/10.1016/j.biochi.2019.11.016
Jarc, E., Petan, T. (2019). Lipid Droplets and the Management of Cellular Stress. The Yale journal of biology and medicine 92(3), 435-452. https://www.ncbi.nlm.nih.gov/pubmed/31543707